Faraday: la materia como manifestación de la fuerza
Por desgracia, conozco bastante bien casos en que la unión de dos seres que parecía íntimamente indisoluble quedó suprimida por la asociación ocasional de una tercera persona, y uno de los que antes estaban tan hermosamente unidos, quedó así expulsado. Entonces los químicos son mucho más galantes –dijo Eduardo–: añaden un cuarto elemento, para que no se produzca ningún vacío.
J. W. Goethe, Las afinidades electivas
 Michael Faraday (1791-1867)
Michael Faraday (1791-1867)

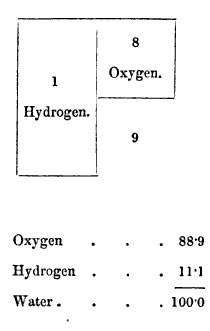 Descomposición del agua mediante el paso de la corriente eléctrica. Faraday, "Course of six lectures on the various forces of matter" (1860)
Descomposición del agua mediante el paso de la corriente eléctrica. Faraday, "Course of six lectures on the various forces of matter" (1860)
 Electroimán: electricidad y magnetismo interconectados
Electroimán: electricidad y magnetismo interconectados
Apuntamos más arriba la importancia que la pila eléctrica había jugado como palanca para romper las sustancias compuestas, haciendo pasar corriente por ellas, y conseguir así incrementar la nómina de elementos descubiertos. Queremos ahora detenernos en otra de las consecuencias que generó el uso de la electricidad como herramienta de investigación en Química.
En efecto, la capacidad de la electricidad para romper las uniones entre los elementos que forman un compuesto sugirió que la misteriosa afinidad química – término con el que se acuñó la mayor o menor capacidad de una sustancia para unirse a otra en los distintos compuestos– además de alimentar la fabulación literaria de románticos como Goethe, quien en su obra Las afinidades electivas, de la que hemos citado un fragmento, la utilizó como recurso para desarrollar una historia de amores y desamores, quizás tuviera que ver con las fuerzas de repulsión y atracción eléctrica: la investigación sobre la naturaleza de los fluidos eléctricos se entrelazó con la investigación química. Una pléyade de científicos famosos pasó así a ocuparse de un tema en el que, en ocasiones de forma explícita y en otras de modo más soterrado, es perceptible un recurrente leit-motiv: la búsqueda de una explicación unitaria de las fuerzas eléctricas y las fuerzas químicas.
En el caso de Faraday, cuyas investigaciones sobre la electrolisis jugarían un papel fundamental en esta búsqueda, la apuesta unitaria llegará incluso mucho más lejos llegando a afirmar:
Es probable que todos los efectos que dependen de las propiedades de la materia inorgánica, incluso la mayoría de los relacionadas con la vida vegetal y animal, dependen en última instancia de la electricidad.
A pesar de que la apuesta del científico inglés, reduciendo la materia, y más en concreto las partículas, a simples zonas de acumulación de fuerzas, resultaría ser excesivamente radical su objetivo último no nos resulta extraño pues en él reconocemos de forma nítida, aunque bajo nuevos rasgos, el sueño de una unificación total. De acuerdo con sus concepciones todo el mundo físico está constituido por una red de líneas de fuerza y el mundo de apariencias que observamos no es otra cosa que una manifestación de las distintas configuraciones de ese entramado de líneas de fuerza que subyace oculto e impenetrable a nuestra observación. De ahí que, a su juicio, todas las fuerzas –eléctricas, químicas, magnéticas o de cualquier otro tipo–, cuya manifestación aparentemente diversa experimentamos, puedan convertirse las unas en las otras.
Resulta paradójico, sin embargo, que fueran los propios trabajos de Faraday los que pusieran de manifiesto las primeras evidencias de la atomicidad de la carga eléctrica. En efecto, las leyes de la electrolisis –descomposición química producida por la corriente eléctrica– permitían establecer relaciones cuantitativas entre la cantidad de sustancia que se descomponía y la cantidad de electricidad que atravesaba la solución. Faraday, de hecho, midió la cantidad de electricidad que se requería para liberar por medio de la corriente un gramo de varias sustancias concretas y halló que la cuantía estaba relacionada con el peso atómico de la sustancia. La búsqueda de una explicación a un nivel más profundo sugería la existencia de una unidad fundamental de carga eléctrica asociada a cada átomo: el electrón se vislumbraba en el horizonte y con él la atomicidad de la carga.
Sin embargo, Faraday, pese a expresarse en estos términos:
Si adoptamos la teoría atómica o su fraseología, entonces los átomos de cuerpos que son equivalentes en su acción química ordinaria tienen las mismas cantidades de electricidad asociadas a ellos de forma natural,
seguiría manteniendo sus reservas y añadiría a continuación:
Debo confesar que me siento incómodo con el término átomo, ya que aunque resulte muy fácil hablar de ellos, resulta muy difícil formarse una idea clara de su naturaleza, especialmente cuando tomamos en consideración cuerpos compuestos.
Los tiempos aún no estaban suficientemente maduros para una cosecha que, aunque se anunciaba, requería de otros operarios.
Actividades
- Explica cuáles son las leyes de la electrolisis
- ¿Qué buscaba Faraday en su estudio sobre las fuerzas eléctricas y magnéticas?